第11回「ヒトの脳画像データベースの構築と統合」
はじめに:疾患と脳画像
高齢化社会の本格化とともに,アルツハイマー病をはじめ脳の老化に起因する認知症性の疾患が急増している.また,現代社会の諸問題を投影する統合失調症やうつ病(気分障害)などの精神疾患の増加も深刻な問題となっている.これらの神経疾患あるいは精神疾患に対する抜本的な対策,また,根本的な治療法の開発にあたっては,動物などを用いた実験的な研究には限界があり,ヒトにおける診断法および評価法の確立が重要である.従来から用いられてきた方法である被験者へのインタビューによる記憶など認知機能の検査は,検査回ごとの変動が大きく,また,その利用は認知症の症状が顕在化した進行期にかぎられることから,今後の新規の治療法の開発や早期また予防的な治療の導入にむけ,発症前の病態を客観的にとらえることのできる脳画像によるバイオマーカーの重要性が高まっている.
脳画像は形態画像と機能画像とに大別される.形態画像の取得には磁気共鳴撮像法(magnetic resonance imaging:MRI)があり,たとえば,アルツハイマー病の進行にともなう脳の海馬領域の萎縮などを評価するために用いられている.機能画像の取得には単光子コンピューター断層撮像法(single photon emission computed tomography:SPECT)や陽電子放射断層撮像法(positron emission tomography:PET)がある.特定の脳の領域に集積するような化合物を放射性同位体により標識したうえで被験者に注入し,この放射性同位体が放出する放射線を捕捉することで化合物の脳における分布や時間変化を画像化し対象領域の機能を解析するものである.標識の対象としてグルコースやアミロイドに結合する化合物などが用いられ,それぞれ,血流量およびグルコースの代謝量,アルツハイマー病の原因タンパク質であるアミロイドβタンパク質の挙動を解析することができる.また,機能的磁気共鳴画像法(functional magnetic resonance imaging:fMRI)は高い空間分解能と時間分解能をもち,被験者へ放射性化合物を注入することなしに脳における血流の変化を測定できる.さらに,拡散テンソル画像(diffusion tensor image:DTI)などの新しい形態画像技術では白質線維の微細な質的および量的な変化をとらえることができる.このようなさまざまな手法で測定された脳画像に対しコンピューターにより画像のむらやゆがみなどの補正処理を行うことにより,複数の画像を統計的に比較することが可能になる.くわしくは,解説書などを参考にされたい[1][2].
1.国外の研究プロジェクト
このように脳画像を用いた疾患の研究には,臨床心理学,放射線医学,画像工学,統計学,データ交換やデータベース構築などの情報科学技術など,分野横断的な人材や技術,情報の結集が必要である.
2001年,米国NIH National Center for Research Resourcesからの助成を受けて,医学研究を支援するためのコンソーシアムであるBIRN(Biomedical Informatics Research Network,URL:http://www.birncommunity.org/)が発足した.米国の大学や研究機関を高速ネットワークにより接続し,データベースやソフトウェアの開発および提供を行っている.このインフラのもと全米10か所以上の大学および研究機関が連携し,アルツハイマー病や統合失調症を対象とした大規模な画像研究も推進され,近年,その成果が報告されている.
国際的には,2002年の経済協力開発機構ワーキンググループの提言にもとづき,2005年に,International Neuroinformatics Coordinating Facility(INCF)が設立され,2011年11月現在,わが国を含む16か国が参加している.
アルツハイマー病に関しては,2004年,米国においてNIHや製薬企業の支援のもと,大規模な臨床研究であるADNI(Alzheimer's Disease Neuroimaging Initiative,URL:http://www.adni-info.org/)が開始された[3].健常な高齢者(200名),軽度の認知障害者(400名),軽症のアルツハイマー病患者(200名)を対象に,心理検査による記憶および各種の認知機能の評価,MRIによる形態画像の検査,PETによる機能画像の検査,脳脊髄液および血液におけるアルツハイマー病の関連物質や遺伝子型の測定などを,半年から1年ごとに最大3年間にわたり実施し,アルツハイマー病の発症を予測するような画像およびバイオマーカーを確定しようとするプロジェクトである.米国California大学のLONI(Laboratory of Neuro Imaging,URL:http://www.loni.ucla.edu/)を中心に,多くの施設において複数の機種により撮像されるMRI画像およびPET画像について,統計学的に相互の比較が可能となるよう撮像,装置の較正,画像処理のプロトコールの標準化が行われ,解析ツールや生データならびに解析後のデータがデータベースLONI Image Data Archive(URL:https://ida.loni.ucla.edu/)から公開されている.北米(NA-ADNI)を中心に,日本(J-ADNI),欧州(E-ADNI),オーストラリア(AIBL),そして,これから活動を開始する予定の台湾(TW-ADNI),韓国(K-ADNI)が連携し研究を行っている(World Wide ADNI:WW-ADNI).さらに,米国では2010年から,アルツハイマー病の発症前診断の可能となるバイオマーカーを探索するべく,5年間の後継プロジェクトADNI-2が開始している.
2.わが国におけるJ-ADNI臨床研究と包括脳ネットワーク
国内に目をむけると,J-ADNI臨床研究(URL:http://www.j-adni.org/)がNA-ADNIに準拠したデザインをもって2007年度より5年間の計画で実施されている.全国で600名の被験者(健常な高齢者150名,軽度の認知障害者300名,軽症のアルツハイマー病患者150名)を募集し,2年間から3年間にわたり,半年から1年の間隔で検査を行っている.認知症およびアルツハイマー病に関する全国38か所の代表的な医療機関において取得されたデータは,個人が特定されないよう匿名化処理され,安全な専用回線を経由してJ-ADNIシステムに集められ管理されている.心理検査,MRI検査,PET検査,生化学検査など,複数の研究チームが連携し,高品質の画像からバイオマーカーを探索するため,撮像や装置の較正におけるノウハウの蓄積や,画像処理や統計処理の技術開発が行われている.MRI画像の補正には独自の手法を採用している.
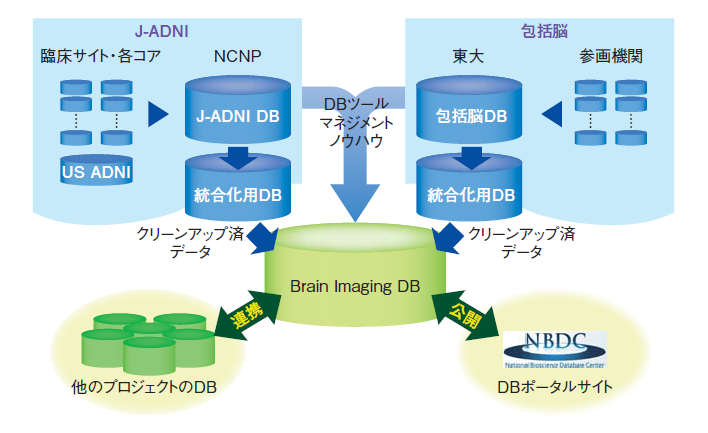
精神疾患に関しては,文部科学省の新学術領域研究「包括型脳科学研究推進支援ネットワーク」(包括脳ネットワーク,URL:https://www.hokatsu-nou.nips.ac.jp/)において2011年度からの3年間で,精神疾患の患者(発達障害,気分障害,統合失調症)ならびに若年の健常対照者について,脳のMRI画像(MRI形態画像,fMRI画像,DTI画像)とそれに付随する臨床情報のデータベースを構築し公開する計画になっている.精神疾患の観点からデータベース構築の意義や目的が検討されており[4],アルツハイマー病と共通する部分も多い.この両者は,バイオサイエンスデータベースセンターの統合化推進プログラムにおいて,統合-脳画像データベース(Brain Imaging DB)を構築し公開することになっている[5].(図1)
3.脳画像データベースの構築
脳画像の解析はMRIやPETを所有する病院や研究所の単位でさかんに行われているが,それでは症例研究の域からでることに困難が生じ,また,データの再利用も重視されていない.一方で,全国レベルや国際レベルでの研究では,画像の補正および標準化が解析に必須になってくる.また,厖大なデータには再利用の価値が高い.そこで,これらのデータベース化が重要となる.画像情報には付加情報として撮像条件(機器,プロトコール)や画像以外の臨床データなど膨大な情報があり,画像にもMRI画像やPET画像など異なる性質のものがある.これらをプロジェクトごとにまとめて管理し解析するため,既存のリレーショナルデータベースと画像ファイルの管理とを組み合わせて構築しなくてはならない.画像フォーマット,補正データとの連携,MRI画像とPET画像との関連,解析結果の表示など,情報を染色体のうえに配置することのできるゲノム情報とは異なり,脳画像のデータベース化はまだ多くの技術的な課題をかかえている.これらを解決しながら解析に用いやすいデータベースを構築することをめざす必要がある.脳画像を扱うプロジェクトにおいては,このようにデータベースの構築が研究の前提となっている.
4.脳画像データベースの統合
医療機関の臨床現場において被験者を長期間にわたり定期的に検査し質の高いデータを得ることは,多くの関係者の厚意や労力のうえに成り立っている.J-ADNIにおいても,600名の検体を全国38か所という多くの施設において収集していることからも,そのとりまとめにさまざまな困難がつきまとうことは想像にかたくなく,集められた高品質の臨床データはきわめて貴重である.大規模かつ再利用の可能な高品質の脳画像データベースによりもたらされる恩恵にはさまざまなものがある.サンプル数が多いほど統計処理の誤差も小さくなるし,将来,健常者データをほかのプロジェクトで再利用することも可能になるかもしれない.疾患の再分類により,より的確な診断やバイオマーカーの発見につながる可能性もある.将来的に最新技術により再解析することで新たな知見の得られる可能性もある.J-ADNIにおいても,apoE遺伝子などリスク遺伝子の多型と,アルツハイマー病の原因タンパク質であるアミロイドβタンパク質の蓄積との相関が研究されているが,さらにふみこんで,さまざまなオミックスデータやシステムバイオロジーと融合し,分子レベルで脳疾患の発症機構を詳細に解明していくという期待ももたれる.アルツハイマー病と精神疾患との病態機構における関係もみえてくるかもしれない.このようななか,異なる種々の疾病の脳画像データの統合が必要となってくる.しかしながら,異なる脳画像をどのように比較し検索するのかなど技術的な課題は山積しており,ひとつひとつ解決しながらデータベースの構築を行う必要がある.一方で,幅広くデータを統合するだけでなく,データの信頼性も重要である.画像データそのものにくわえ,それに付随する被験者の情報や撮像の条件などいわゆるメタデータも整備しなければならない.
従来,データベースの構築はひとつの研究プロジェクトの後始末に近い位置づけであったが,このように膨大なデータを創出する研究プロジェクトでは,データベースの構築そのものがひとつの大きな成果であり,つぎのプロジェクトをデザインするうえでも貴重な基礎資料となるものである.したがって,有用性の高いデータベースの構築のためには,情報技術的な観点でのデータベースの設計やGUI(graphical user interface,グラフィックス表示やマウスなどポインティングデバイスを用いた,直観的なソフトウェアの操作体系)の使い勝手などの議論だけではなく,研究者とコミュニケーションをとり,分野横断的な視点からデータの産出された背景やその意味を理解できる人材が必要とされている.
おわりに:将来の展望
2000年にヒトのDNA全塩基配列が明らかにされ,多くの遺伝子の機能が明らかにされてきたが,脳の研究はその高次機能ゆえに緒についたばかりであり,遺伝子と機能との関係もモデル生物において進んでいる段階である.しかしながら,脳の機能を測定するための技術開発はめざましく進んでおり,疾患の脳画像データベースの構築はアルツハイマー病や統合失調症などの疾病の本質を明らかにし,さらに,治療薬の効果を臨床治験により評価していくためのインフラの構築として,きわめて重要なものと位置づけられる.将来的には,ここにオミックスの情報やモデル生物の知見などが有機的に統合されて,新たな発見の場となることも期待される.画像の解析においても,今後,さまざまなツールの開発が必要である.これらの理由から,良質かつ将来のどのような用途にも対応できるようなデータベースの構築が必要である.
参考文献
- 松田博史, 朝田 隆 編: 見て診て学ぶ認知症の画像診断 改訂第2版. 永井書店 (2010) ↑
- 核医学文献情報研究会: ミスターPETの核医学教室. http://www.asca-co.com/nuclear/ ↑
- Weiner, M. W., Veitch, D. P., Aisen, P. S. et al: The Alzheimer's Disease Neuroimaging Initiative: a review of papers published since its inception. Alzheimers Dement., 8, S1-S68 (2012) ↑
- 八幡憲明, 根本清貴, 山下典生: 精神疾患の脳画像データベース構築に向けて. 医学のあゆみ, 231, 991-995 (2009) ↑
- 岩坪 威: ヒト脳疾患画像データベース統合化研究. http://biosciencedbc.jp/gadget/rdprog_over/iwatsubo.pdf ↑
↑ 押下で本文に戻ります。
本稿作成にあたり貴重な助言を頂戴した三橋信孝(バイオサイエンスデータベースセンター)、長洲毅志(エーザイ株式会社)の両先生に深謝いたします。

Licensed under a Creative Commons 表示2.1日本 license ©2012 八幡憲明(東京大学大学院医学系研究科)、笠井清登(東京大学大学院医学系研究科)、岩坪 威(東京大学大学院医学系研究科)
なお、本記事は細胞工学2012年4月号掲載の原稿を改変したものです。